אִבחוּן
תסמונת Wellens מסוג A
מה לעשות אחר כך
ג בצע אנגיוגרפיה כלילית
המפתח לאבחנה הנכונה הוא ההכרה שגל T הדו-פאזי ב-Leads V2 ו-V3 ב-ECG בחולה עם כאבים בחזה לאחרונה עשוי לרמז על חסימת עורקים כליליים קרובה. שחרור הביתה (בחירה A) אינה מומלצת, ואקו-לב דובוטמין (בחירה C) אסורה בחולים עם אנגינה לא יציבה מתמשכת. בחירה D אינה נכונה מכיוון שבהתבסס על ממצאי א.ק.ג אלו, יש לבצע אנגיוגרפיה כלילית ללא קשר לרמות הטרופונין בדם.
דִיוּן
תסמונת וולנס מייצגת דפוסים ספציפיים של גלי T ב-EKG המתקבלים במהלך מרווח ללא כאבים בחזה שעלול לבשר על התפתחות של אוטם שריר הלב.1 תסמונת וולנס נמצאת ב-5.7% מהחולים עם תסמונת כלילית חריפה (ACS)2 ו-8.8% מהחולים מטופלים עם אוטם שריר הלב ללא ST-elevation (NSTEMI) שעוברים אנגיוגרפיה כלילית.3 בקרב מטופלים עם NSTEMI, אלו עם תסמונת Wellens נוטים פחות לסבול מהיסטוריה של מחלת לב כלילית או התערבות מלעורית קודמת (PCI) מאשר אנשים ללא Wellens .2
קריטריונים אבחוניים לתסמונת ולנס כוללים הפרעות בגלי T טרום-קורדיאלי עם מקטעי ST איזואלקטריים או מוגברים (<1 מ”מ), היעדר גלי Q טרום-קורדיאליים, אנגינה לאחרונה וסמני סרום לב נורמליים או מוגברים.4 תסמונת Wellens מסוג A מאופיינת על ידי גלי T דו-פאזיים ב-V2 ו-V3.2,4,5 מובילים בתבנית מסוג B הם בעלי גלי T סימטריים והפוכים עמוק ב-V2 וב-V3, ומדי פעם ב-V1, V4, V5 ו-V6, והוא נראה ב-70% מהחולים עם תסמונת וולנס.2,4,5 הפרעות בגלי T עשויות לנבוע מאפיזודה קצרה של איסכמיה בשריר הלב עקב קרע רובד בעורק הכלילי שחולף לאחר פרפוזיה ספונטנית.3,6 בצקת בשריר הלב עשויה גם לתרום לפתופיזיולוגיה של תסמונת וולנס.7
האבחנה המבדלת עבור חולים עם היסטוריה של כאבי חזה וגלי T לא תקינים ב-ECG כוללת איסכמיה חריפה של העורקים הכליליים, דיסקציה של העורקים הכליליים או וסוספאזם, תסמונת טקוטסובו, גישור שריר הלב, קרדיומיופתיה של חדר ימין או היפרטרופי, תסחיף ריאתי,5, 4. ,7
תסמונת Wellens תוארה לראשונה ב-26 אנשים עם אנגינה לא יציבה.1 למרות טיפול רפואי מיטבי, 8 מתוך 9 החולים שלא עברו אנגיוגרפיה לבבית מוקדמת פיתחו אוטם שריר הלב בדופן הקדמית בממוצע של 8.5 ימים לאחר האשפוז בבית החולים. לעשרה מתוך 11 החולים שעברו אנגיוגרפיה לבבית מוקדמת (ממוצע של 4 ימים לאחר האשפוז) היו לפחות 90% היצרות של העורק היורד הקדמי (LAD).1 סדרות גדולות יותר ויותר עדכניות דיווחו על נגע יחיד ב-LAD ב-35% עד 67% מהחולים, 3,4,6 עזבו היצרות של העורק הכלילי הראשי ב-5% עד 12.7%, 4,6 מחלה מרובה כלי דם ב-30%,6 ומחלה כלילית רגילה או לא חסימתית ב-25% עד 30%.3-5
למטופלים עם תסמונת וולנס שעוברים אנגיוגרפיה כלילית יש שיעור תמותה קרדיווסקולרית למשך 6 חודשים של כ- 5%.6 בהשוואה לחולים אחרים שטופלו באנגיופלסטיה בשל נגע LAD האשם, לאנשים עם תסמונת וולנס אין סיכון מוגבר למוות מכל הסיבות. , מוות לבבי, MI חוזר, revascularization של הנגע ושבץ לאחר 24 חודשים.2
הכרה מיידית של תסמונת וולנס וריוסקולריזציה מוקדמת של כלי הדם הכליליים עם PCI או השתלת מעקפים של העורקים הכליליים עשויים להפחית תחלואה ותמותה על ידי מניעה או הגבלת אוטם שריר הלב.
תוצאה של מטופל
ב-ED, למטופל נרשמו 300 מ”ג של חומצה אצטילסליצילית (אספירין) ו-5000 U של הפרין תוך ורידי. אקו לב ליד המיטה גילה היפוקינזיס קדמי קל עם שבר פליטה של 50%. בדיקות דם חוזרות ב-ED גילו רמת טרופונין T של 10 ng/mL, אשר ירדה מ-16 ng/mL שעה אחת לפני כן. צנתור לב, שבוצע 4 שעות לאחר הגעת ED, חשף חסימת LAD פרוקסימלית תת-סכמית עם מעורבות של העורק הכלילי הראשי השמאלי (איור 2). לא בוצעה התערבות, והמטופל טופל באספירין, רוסווסטטין ובמינון מניעתי של הפרין במשקל מולקולרי נמוך. ארבעה ימים לאחר מכן, הוא עבר ניתוח מינימלי פולשני ישיר מעקף עורקים כליליים (MIDCAB) עם אנסטומוזה של עורק החלב הפנימי השמאלי ל-LAD.
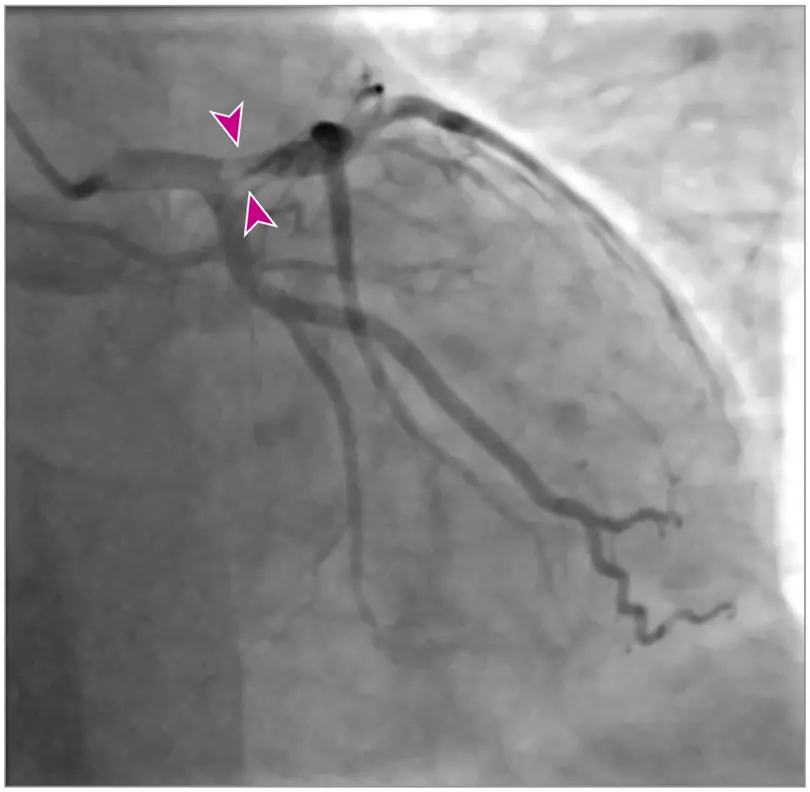
חסימה פרוקסימלית חמורה (ראשי חץ) של העורק היורד הקדמי השמאלי קרוב לעורק הכלילי הראשי השמאלי.
אקו לב טרנס-חזה שבוצע 6 ימים לאחר ניתוח לב הדגימה שבר פליטה של 65%. המטופל שוחרר מבית החולים 11 ימים לאחר האשפוז ונרשם לו אספירין, clopidogrel, metoprolol, rosuvastatin ו-pantoprazole. בביקור במרפאת חוץ 4 שבועות לאחר השחרור מבית החולים, החולה היה א-סימפטומטי, הפסיק לעשן, והאק”ג שלו הראה רזולוציה של גלי T דו-פאזיים ב-V2 ו-V3.
Corresponding Author: Christian Oeing MD, Department of Internal Medicine and Cardiology, Charité-University Medicine Berlin, Campus Virchow Klinikum, Berlin, Germany (christian.oeing@charite.de).
Published Online: October 31, 2022. doi:10.1001/jama.2022.19443
Conflict of Interest Disclosures: None reported.
Additional Contributions: We thank the patient for granting permission to publish this information.
